Accueil > Équipes scientifiques > Structure et dynamique des systèmes complexes isolés photoexcités (SYSIPHE) > MEcanismes MOléculaires d’espèces biomimétiques (MEMO) > Etude dynamique photoinduite et conformationnelle de modèles de biomolécules
Etude dynamique photoinduite et conformationnelle de modèles de biomolécules
par - 12 octobre 2020 (modifié le 13 octobre 2020)
Les biomolécules sont des molécules complexes, pouvant généralement adopter de nombreuses conformations (différents arrangements de la molécule dans l’espace) et être le sein de nombreuses voies d’excitation et relaxation électronique après absorption d’un photon. Nous nous intéressons aux processus dynamiques ultrarapides (ps ou fs, c’est-à-dire 10-12 ou 10-15 s) tels que le transfert d’un électron d’un atome à un voisin (transfert de charge) ou passage d’un état singulet (spin = 0) à un état triplet (spin = 1). Afin de pouvoir étudier efficacement les mécanismes ou interactions en jeu, nous étudions des systèmes modèles de ces molécules biologiques et principalement en phase gazeuse (isolée de tout solvant) ou micro-solvatée (une ou quelques molécules d’eau).
Ainsi, nous avons entamé une étude des processus physiques induits dans le cadre de la photothérapie dynamique, qui est une alternative peu ou pas invasive et non toxique dans le traitement du cancer basée sur la photoexcitation d’un photosensibilisateur, souvent un dérivé métalloporphyrinique, sélectif d’un récepteur moléculaire qui sert à former de l’oxygène singulet par transfert d’énergie. L’oxygène singulet est une espèce très réactive et sera, in fine, l’agent thérapeutique. Les trois axes de cette étude sont donc 1) L’étude du réarrangement électronique ultrarapide au sein de la métalloporphyrine après absorption d’un photon, 2) L’étude du transfert d’énergie entre la métalloporphyrine excitée et le dioxygène et 3) L’étude de la reconnaissance de forme entre le photosensibilisateur et un récepteur moléculaire.
1) Réarrangement électronique au sein de la métalloporphyrine
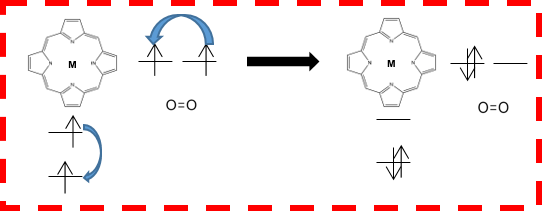
Après excitation de la métalloporphyrine vers l’état électronique excité S1 ou S2, elle se relaxe par croisement intersystème vers l’état triplet T1 qui est l’état à longue durée de vie dans lequel l’interaction avec le dioxygène est possible. En fonction du métal au centre les durées de ces réarrangements électroniques sont très variables (voir J. Chem. Phys. 124, 114302, 2006) et le passage de l’état électronique excité S1,2 vers l’état métastable T1 est encore sujet à interprétation. Plus précisément, il est possible que dans le cas de métaux de transition, il y ait passage par un état à transfert de charge (un électron de la porphyrine est transféré au métal) (voir par exemple J. Phys. Chem. A 2013, 117, 8111-8118) mais ce type d’état est particulièrement délicat à mettre en évidence expérimentalement. Pour ce faire nous mettons en place une nouvelle méthodologie basée sur des expériences ultrarapides dites pompe-sonde où un faisceau laser (le faisceau pompe) permet d’exciter la transition électronique vers l’état S1,2 et un autre (le faisceau sonde) viendra ioniser la molécule en arrachant un électron interne du métal permettant d’avoir une image instantanée de l’état électronique de la métalloporphyrine grâce à une sonde locale (le métal au centre). Les expériences sont réalisées sur des grands instruments (Lasers à électrons libres, synchrotrons) et des sources lasers ultrarapides : les sources d’harmoniques d’ordre élevé.
2) Transfert d’énergie au dioxygène environnant
Le mécanisme régissant le transfert d’énergie entre la métalloporphyrine excitée et le dioxygène est encore sujet à débat. De nombreuses études ont été menées sur des molécules organiques dans les années 70 (!) sans qu’un consensus n’ait été trouvé. L’hypothèse nous semblant la plus robuste est qu’il y a formation d’un intermédiaire réactionnel. Pour le mettre en évidence, un dispositif expérimental, actuellement en cours de montage, contenant une source à électrospray et un piège à ions nous permettra de piéger les métalloporphyrines dans un état ionique suffisamment longtemps pour pouvoir sonder leur interaction avec du dioxygène qui sera introduit dans le piège. En faisant varier la température dans le piège, nous pourrons déterminer la constante cinétique de la réaction (loi d’Arrhénius) et donc déterminer le type de mécanisme à l’œuvre. Grâce à des expériences pompe-sonde, nous pourrons également mesurer l’efficacité relative de passage à l’état triplet des métalloporphyrines en fonction du métal situé au centre.
3) Reconnaissance photosensibilisateur/récepteur moléculaire
Afin d’améliorer le ciblage de récepteurs sur les cellules tumorales, une voie d’étude porte sur l’ajout de sucres sur les métalloporphyrines (voir https://www.photoniques.com/articles/photon/pdf/2017/01/photon201785p17.pdf). En effet, parmi les nombreuses fonctionnalités des sucres in vivo, ils sont notamment connus pour être moteur dans la reconnaissance moléculaire. Le but de cette partie est de comprendre les interactions entre des sucres et des peptides (systèmes modèles des récepteurs des cellules tumorales) par spectroscopie IR en phase gazeuse. Les expériences réalisées sont complémentées par une approche théorique –aussi réalisée dans l’équipe- basée sur des méthodes de machine learning pour faire le tri parmi toutes les conformations possibles et des calculs de chimie quantique pour pouvoir simuler les spectres et les comparer aux résultats expérimentaux.
L’équipe a formé de nombreuses collaborations nationales et internationales parmi lesquelles : l’équipe DIRAM à l’ISMO, l’équipe de relaxation de molécules excitées en couche interne du LCPMR, les équipes structures biomoléculaires et dynamique réactionnelle du LIDYL (CEA), le groupe Weinelt de la Freie Universität à Berlin, le groupe Strong Field Processes at Extreme Wavelengths du Max-Born Institute à Berlin.