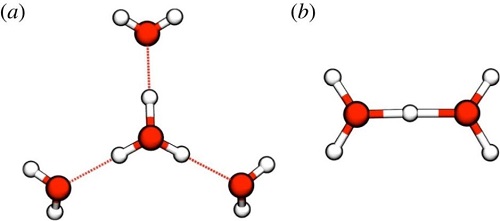
Malgré son importance considérable, le mécanisme « de Grotthus » par lequel un proton en « excès » ou en défaut en solution aqueuse se transmet à travers les liaisons hydrogène des molécules d’eau demeure très largement incompris. Dans l’eau liquide, la solvatation de ces protons en excès est représenté sous deux formes principales : H9O4+ (cation Eigen) et H5O2+ (cation Zundel). Très récemment, des travaux expérimentaux ont conclu que le cation Zundel serait la forme prédominante mais des simulations encore plus récentes semblent indiquer que c’est, au contraire, le cation Eigen qui domine.
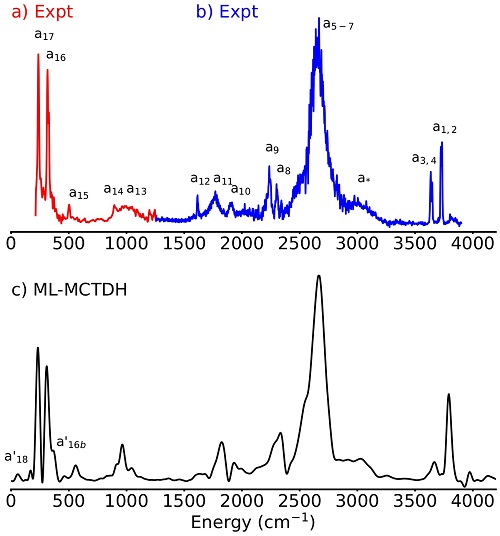
Des calculs quantiques en dimension complète (jusqu’à 33 dimensions) basés sur la méthode Multi-Layer Multi-Configuration Time-Dependent Hartree (ML-MCTDH) ont permis de reproduire correctement les spectres Infra-rouges des cations Zundel et Eigen. Ces calculs ont permis une compréhension fine des couplages entre le proton et les molécules d’eau qui l’entourent dans sa première couche de solvatation. La conclusion est que l’entité H5O2+ est l’unité fondamentale qui permet d’expliquer les deux spectres. En effet, le spectre du cation Eigen peut être expliqué par H5O2+ polarisé par les deux autres molécules d’eau. Ces dernières n’ajoutent pas de couplage dynamique supplémentaire.
Ces résultats expliquent en partie pourquoi il est si difficile de déterminer les rôles respectifs des deux cations : en effet, H5O2+ (le cation Zundel si H5O2+ est isolé) a des propriétés spectroscopiques similaires au cation Eigen lorsqu’il est dans un milieu polarisé. D’autre part, le fait que le cation Eigen puisse être rationalisé comme H5O2+ polarisé par deux molécules d’eau confirme la possibilité du processus dit de la « danse spéciale de paire » où l’énergie du H+ est transférée très rapidement d’une paire de molécule d’eau à une autre, les trois paires jouant des rôles symétriques.
Contact : Fabien Gatti
Schröder, M., Gatti, F., Lauvergnat, D. et al. The coupling of the hydrated proton to its first solvation shell.
Nat Commun 13, 6170 (2022)